Una pieza esencial de la división celular sale a la luz
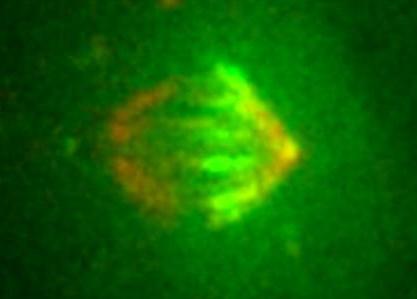
Un avance del IRB Barcelona llena un vacío fundamental de conocimiento sobre la formación del aparato principal de la división celular, el huso mitótico.
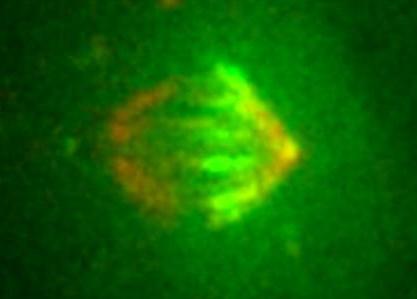
La visualización y seguimiento en vivo de los extremos iniciales de los microtúbulos, filamentos que organizan el huso mitótico, ofrece una imagen más comprensible de su arquitectura dinámica.
Los resultados también ayudarán a entender cómo actúan fármacos usados en quimioterapia cuyo blanco son los microtúbulos.
Para cada división de una célula en dos se ensambla una estructura extremadamente compleja, el huso mitótico, resultado de la acción coordinada y finamente equilibrada de multitud de proteínas. Buena parte del tiempo que invierte una célula en dividirse lo dedica a ensamblar y poner a punto esta pieza principal de la división, que se asemeja superficialmente a una pelota de rugbi.
El componente más abundante del huso son los microtúbulos. “Miles de ellos”, explica el biólogo celular del Instituto de Investigación Biomédica (IRB Barcelona), Jens Lüders, “filamentos finos, imprescindibles y extremadamente dinámicos y cambiantes, a los que al fin, hemos podido marcar en su extremo inicial y seguir su localización y movimiento durante el ensamblaje y arquitectura del huso mitótico”. El avance lo publicó este domingo por la tarde la revista Nature Cell Biology en edición online avanzada.
“Durante más de 10 años sólo hemos podido rastrear los finales de los microtúbulos pero no había nada para los inicios lo que suponía un cuello de botella para la investigación del huso mitótico y para entender mejor su función en la división celular”, describe Lüders. El científico alemán es el jefe del grupo Organización Microtubular en el IRB Barcelona, y ha tutelado el estudio que lleva únicamente dos nombres, el suyo y el del francés Nicolas Lecland, primer autor, quien ha desarrollado su doctorado con una beca de “la Caixa” en el IRB.
Los científicos han conseguido demostrar que la proteína gamma tubulina (γ-tubulin) se localiza en los inicios de los filamentos microtubulares y se mantiene relativamente estable asociado a estos. Después han preparado un marcador fluorescente que se adhiere a γ-tubulin y que activan mediante foto activación por láser para filmar en vivo la evolución de los extremos iniciales de los microtúbulos en el huso mitótico de células humanas en división. En la puesta a punto de la tecnología ha sido clave la Plataforma de Microscopía Digital Avanzada compartida por el IRB Barcelona y el Parque Científico de Barcelona, y que está dirigida por el físico francés del IRB, Julien Colombelli. “El éxito del trabajo se debe también a los conocimientos técnicos y las tecnologías de punta que tenemos al alcance y sin las cuales no nos podríamos haber planteado este proyecto”, enfatiza el científico.
Los investigadores describen por primera vez dónde se generan dentro del huso la mayor parte de los microtúbulos, cómo evolucionan y cómo se transportan mediante la acción de tres proteínas motor, hacia los polos opuestos de la célula, donde se anclan.
Simultáneamente a este proceso, los extremos opuestos de los filamentos se alargan hacia el centro de la célula donde interactúan con los cromosomas. Cuando el huso esté finalmente dispuesto, los microtúbulos tirarán de los cromosomas para iniciar la división. “Ahora tenemos una visión más completa de la dinámica del huso y de cómo funciona, y podremos usar nuestro nuevo marcador para testar viejas y nuevas hipótesis sobre los mecanismos subyacentes”, subraya el investigador.
Una nueva herramienta para el estudio del cáncer
El avance abre además la puerta a comprender mejor el modo de acción de fármacos usados en quimioterapia que tienen como diana a los microtúbulos. Este tipo de fármacos perturban la formación del huso mitótico con la consecuente detención del ciclo celular y por lo tanto interfiriendo en el crecimiento del tumor.
A pesar de los muchos años de éxito clínico de estos tratamientos contra el cáncer apenas se entiende cómo impiden la formación y función del huso. Aunque son fármacos muy eficientes no son todo lo finos que se desearía ya que también afectan a las células sanas en división. Además también afectan a células que no se dividen como las neuronas, en las que los microtúbulos tienen funciones importantes.
“Comprender mejor las diferencias en cuanto a la organización y función del huso mitótico de células tumorales y células sanas y cómo responden ante los fármacos antitumorales es esencial para optimizar los tratamientos, por ejemplo, identificando nuevos fármacos más específicos o nuevas dianas. Esta herramienta puede ser útil a tales propósitos”, anuncia el investigador.
El estudio se ha llevado a cabo gracias a fondos estructurales de la Generalitat de Catalunya, una beca Marie Curie de la Unión Europea y al Plan Nacional del Ministerio de Economía y Competitividad.
Temas relacionados:
También te puede interesar
Esta web se reserva el derecho de suprimir, por cualquier razón y sin previo aviso, cualquier contenido generado en los espacios de participación en caso de que los mensajes incluyan insultos, mensajes racistas, sexistas... Tampoco se permitirán los ataques personales ni los comentarios que insistan en boicotear la labor informativa de la web, ni todos aquellos mensajes no relacionados con la noticia que se esté comentando. De no respetarse estas mínimas normas de participación este medio se verá obligado a prescindir de este foro, lamentándolo sinceramente por todos cuantos intervienen y hacen en todo momento un uso absolutamente cívico y respetuoso de la libertad de expresión.
No hay opiniones. Sé el primero en escribir.